pH值计算器
该在线pH计算器旨在确定给定化合物的水溶液的pH值。您可以从化学品列表中选择任何酸或碱,或使用已知值作为解离常数 K一个或 Kb.物质的浓度可以用摩尔或每单位体积的质量单位来指定。
酸碱度标
在化学方面,pH(表示“氢的电位”或“氢的功率”)是用于指定水溶液的酸度或碱度的定量度量。
pH定义为氢离子活度的负十进制对数,一个H+,在解决方案中:
反过来,氢离子活性取决于氢离子的浓度,氢离子在稀溶液中可以用以下公式表示:
哪里
[H+]是氢离子的浓度,
c0是标准状态浓度c0= 1 摩尔/升。
所以一个H+是一个可以定义对数的无量纲数。在实践中,使用以下公式进行计算pH:
哪里[H+]被认为以摩尔/升为单位给出。
在25°C的纯(中性)水中,氢离子的浓度为10−7摩尔/升。这给了我们一个pH水等于7。中性值pH取决于温度 – 如果温度升高,则低于 7。
具有pH小于 7 被认为是酸性的;具有pH大于 7 被视为碱性或碱性。pH通常范围在 0 到 14 之间。这pH对于非常强的酸,值可以小于 0,对于非常强的碱,值可以大于 14。
同样,我们可以定义pOH作为氢氧根离子浓度的量度,OH−:
由于H+和OH−在纯水中相等,很容易证明在25°C时以下公式是有效的:
如何计算pH值
pH值计算对于强酸和弱酸和碱,溶液的摩尔浓度值是不同的。
强酸和强碱
强酸和强碱是在正常情况下几乎完全在水中解离的化学物质。这意味着酸性溶液中氢离子的浓度可以取为等于酸的浓度。类似地,碱性溶液中氢氧根离子的浓度可以取为等于碱的浓度。
在这种情况下,我们可以使用上述公式pH和pOH通过简单地替换酸和碱浓度而不是[H+]和[OH−]分别。
只有七种酸和只有五种水溶性碱被认为是强的。
弱酸和弱碱
弱酸和弱碱在水中仅部分解离。这使计算复杂化
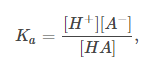
解离常数显示了水溶液的平衡条件:
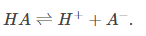
很容易证明,知道解离常数
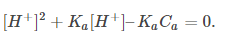
该二次方程的解给出了氢离子浓度,因此
相同的方法适用于碱溶液,只有碱解离常数